Suivi temporel d’une réaction chimique
Synthèse C2
I Suivi
temporel de l’évolution d’un système chimique
Pour suivre l’évolution d’un
système chimique, on trace la courbe d’évolution de l’avancement x en fonction
du temps.
Pour cela on mesure à
différentes dates, la quantité de matière d’un des réactifs ou d’un des
produits par une méthode physique de mesure (spectrophotométrie, mesure de
pression, conductimétrie) ou par une méthode chimique (titrage).
I-1 Le titrage :
Le principe du titrage st de
faire réagir, de manière totale et rapide, l’espèce à titrer avec
l’espèce titrante.
L’équivalence du titrage
correspond au changement de réactif limitant, pour un volume équivalent de
solution titrante ajouté. La connaissance du volume équivalent permet de
déterminer la quantité de matière de l’espèce titrée présente dans
l’échantillon.

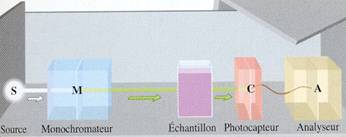
I-2 La
spectrophotométrie
L’absorbance A d’une espèce
représente sa capacité à absorber une radiation de longueur d’onde donnée.
C’est une grandeur sans unité.
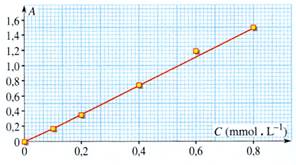
Pour des solutions
suffisement diluées, l’absorbance A d’une espèce absorbante X est
proportionnelle à sa concentration [X]. La relation entre ces deux grandeurs
est donnée par la loi de Beer-Lambert

A = eλ.[X]. l
[X]
est exprimée en mol.m-3 ; l est l’épaisseur de solution
traversée, eλ est un facteur caractéristique de
l’espèce absorbante, dont la valeur dépend de la longueur d’onde en mol-1.m²
Par
suivi temporel de l’absorbance d’une solution, on peut suivre l’évolution de la
concentration en espèce absorbante en cours du temps.
II Vitesse de
réaction
II-1 Définition
·
Pour une transformation se
déroulant dans un milieu réactionnel de volume V constant et modélisée par une
réaction, la vitesse de la réaction est une fonction du temps t vérifiant la
relation.
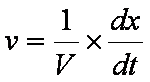
Avec
l’avancement x en mol, t en s, V en L et v en mol.L-1.s-1
·
La vitesse de réaction est une
grandeur positive
·
Pour
une équation chimique aA + bB ® cC + dD, la vitesse de réaction peut s’exprimer en
fonction des concentrations des espèces intervenant dans la réaction :
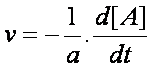 ou
ou 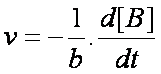 ou :
ou : 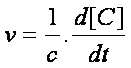 ou
ou 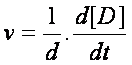
II-2 Mesure sur les
courbes
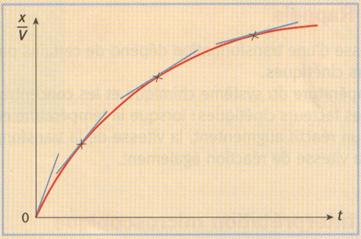
la valeur de la vitesse de réaction à une
instant t est égale à celle du coefficient directeur de la tangente à la courbe
représentant x/V en fonction du temps au point d’abscisse t.
Au cours d’une
transformation, la vitesse de réaction diminue dans la plupart des cas. Elle
tend vers zéro quand t tend vers l’infini.
III Temps de
demi-réaction
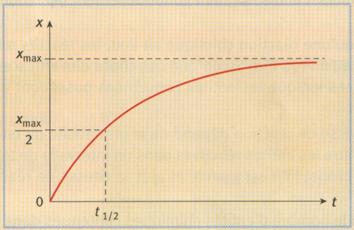
Le temps de demi-réaction,
noté t1/2 , correspond à la durée nécessaire, à partir de l’instant
correspondant à l’état initial dus système, pour que l’avancement de la
réaction soit parvenu à la moitié de sa valeur finale.
JMPodvin Juillet 2002